(Ciencias de Joseleg)(Biología)(Reproducción en los seres
vivos)( Enfermedades reproductivas) (Introducción)(Generalidades)(Introducción
al VIH)(Etapas
de la infección por VIH)(Virus
oportunistas)(Bacterias
oportunistas)(Protistos
oportunistas)(Hongos
oportunistas)(Otros
síntomas del SIDA)(Transmisión
y contagio)(SIDA
infantil)(Taxonomía)(Genética)(Como
ingresa el VIH al cuerpo, tropismo)(Respuesta
inmune)(Ciclo
de vida del VIH)(Diversidad
y adaptabilidad del VIH)(Diagnostico)(Efecto
del VIH en el sistema inmune)(Prevención,
tratamiento y epidemiología del VIH)(Descubrimiento
del VIH y el SIDA)(VIH,
historia y sociedad)(Controversias
sociales y negacionismo del VIH y el SIDA)(Algunas
infecciones de transmisión sexual)(Desordenes
reproductivos masculinos)(Desordenes
reproductivos femeninos)(Referencias
bibliográficas)
El objetivo celular más común y más conocido del VIH es sin duda alguna los linfocitos T efectores o ayudadores, de hecho, es la concentración de linfocitos T la que se emplea para describir la progresión de la infección, la carga viral y en últimas para definir la misma etapa de SIDA. SIDA se define como la etapa de la infección por VIH crónica en la que la concentración de linfocitos T efectores es inferior a 200 células por milímetro cúbico. Lo que no es tan conocido es que el VIH puede atacar a otras células del sistema inmune de forma directa como gran parte del linaje monocitario –léase las dendríticas y los macrófagos –y también es capaz de afectar de forma indirecta a otros componentes del sistema inmune. Adicionalmente, el VIH es capaz de infectar células microgilales. En esta sección examinaremos algunos detalles del tropismo –las líneas celulares que son afectadas por la infección de un virus –del VIH, poniendo énfasis en los mecanismos moleculares que permiten su adhesión e ingreso a la célula blanco.
El estudio del tropismo se centra no solo en los linajes celulares que pueden ser atacados por el VIH, sino también por las causas moleculares –que en últimas son proteínas –que le permiten al virión anclarse en la superficie de una célula e ingresar a ella. Las muestras del VIH-1 fueron clasificadas inicialmente a sus propiedades trópicas, citopáticas y replicativas. Es decir, se basaban de cualidades del virus. El estudio del tropismo a nivel molecular ha permitido clasificar las infecciones del VIH de acuerdo a una nomenclatura sistemática que emerge de los códigos de las proteínas que le permiten ingresar o atacar a una célula.
Figura 36. El VIH solo puede ingresar
a las células que poseen receptores específicos en sus membranas.
El Receptor CD4 es una inmunoglobulina en ramillete que le da su nombre a los linfocitos T efectores o ayudadores, este receptor interactúa con el complejo mayor de histocompatibilidad durante la presentación del antígeno y permite dar inicio a la respuesta inmune humoral y adaptativa.
Figura 37. Receptores y
correceptores. CD4 "rojo" se conecta junto con otros correceptores al
complejo mayor de histocompatibilidad o su homólogo gp120. En la imagen tenemos
a gp120 presentado por el VIH.
CD4 es
una proteína de tipo cuaternario muy alargada que interactúa con el complejo
mayor de histocompatibilidad del tipo II y con el receptor gp120 del VIH. El
nombre CD va por dos rutas, la primera hace referencia a expresión clúster de
diferenciación 4. Clúster de Diferenciación (CD) es un sistema de nomenclatura
para nombrar de forma sistemática las inmunoglobulinas de la superficie, algo
semejante al sistema de nomenclatura IUPAC para sustancias químicas simples.
Por
otro lado, CD también hace referencia a 4 inmunoglobulinas pegadas “de allí la
expresión ramillete y el doble significado de clúster” y una cola
Citoplasmática/intracelular –la C viene de citoplasmática. Las inmunoglobulinas
están codificadas desde D1 hasta D4, donde D1 y D3 son variables mientras que
D2 y D4 son constantes.
El
receptor emplea la porción D1 para interactuar con el dominio beta2 del
complejo mayor de histocompatibilidad del tipo II –por lo cual la inmunidad por
vía del CMH-I no está mediada por este receptor. Aparentemente la proteína de
superficie en VIH llamada gp120 es un homólogo al domino beta2 del complejo
mayor de histocompatibilidad, lo cual le permite al virus anclarse al receptor
CD4 al inicio de su ciclo vital.
Los
primeros estudios de aislamiento del virus del VIH clasificaban las cepas de
acuerdo a su velocidad de infección, por lo cual se empleaban las etiquetas
rápido/lento para distinguir las cepas con alta carga viral y una rápida
progresión a la etapa de SIDA de las cepas con poca carga viral y un lento
progreso a la etapa de SIDA. Otros rasgos que distinguían a las cepas rápidas
de las lentas eran la cinética –velocidad –con la cual los viriones se acoplan
de forma efectiva a la superficie de las células que atacan y la cantidad de
viriones liberados de una célula anfitrión que se encuentra secuestrada y en
proceso de producción de más virus.
Históricamente
las cepas lentas fueron las primeras en ser descritas. Esto se debe a que,
durante una infección por contacto sexual, los mecanismos de infección
generalmente son células dendríticas y macrófagos comunes en las mucosas
sexuales, y los viriones lentos tienden a estar asociados a estas células del
sistema inmune. Con los años y cuando llega la etapa de SIDA la cepa rápida se
desarrolla, lo cual hizo de la descripción de las cepas rápidas fuera más lenta
y/o a que los resultados de las publicaciones parecieran ser incoherentes –lo
cual es aprovechado por los negacionistas del VIH.
En
cualquier caso la respuesta es simple, la velocidad de la infección muta
gradualmente desde lenta y de baja productividad al inicio de la infección a
rápida y de alta productividad en la etapa subclínica y de SIDA.
Otros de los primeros aislamientos, particularmente aquellos obtenidos de individuos en etapa de SIDA, inducían a la formación de sincitios –células polinucleadas mediante la sinapsis viral. Estas cepas fueron clasificadas como formadoras de sincitios (SI por sus siglas en inglés) para distinguirlas de las que no formaban sincitios (NSI por sus siglas en inglés).
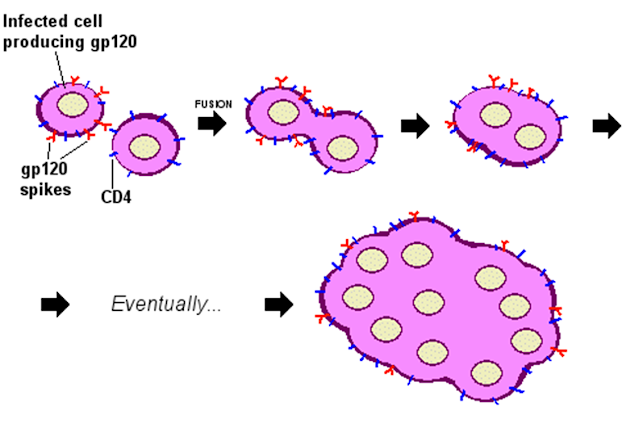
Figura 38. Los sincitios virales. Los
sincitios son células que han mutado por efecto del VIH y los receptores
virales gp120, se forman al fusionar células sanas con infectadas. Algunos
tipos de cáncer también forman sincitios, es un carácter diagnóstico en las
citologías.
El mecanismo
inductor del sincitio son los receptores CD4 y el coreceptor CXCR4. El
coreceptor CXCR4 atrae con más fortaleza cualquier cosa homóloga a una
citoquina y lo ingresa a la célula, lo cual incluye a otras células. Durante la
infección por VIH la proteína GP160 se forma a partir de GP41 y GP120 en la
membrana de la célula infectada, si está célula interactúa con otro linfocito,
primero formando una sinapsis continua y luego haciendo que las dos se fusionen
-en caso de que la cepa que produjo el gp 160 sea afín con CXCR4 -formando una
célula polinucleada llamada sincitio.
Algunas
cepas formadoras de sincitios son capaces de infectar las líneas de células T
CD4+ pero no a los descendientes del linaje de los monocitos –como los
macrófagos y las dendríticas. Estas cepas del VIH fueron designadas como Virus
del linaje de las células T o virus de trofismo de células T. En inglés se las
describe como TCL-trofic pero también se las puede describir simplemente como
T-tróficas tanto en inglés como en español.
Resulta conveniente realizar un breve resumen de los componentes celulares del sistema inmune, para poder tener una visión de cuáles son los tipos de célula que el VIH ataca. Los glóbulos blancos se dividen de polimorfonucleares y mononucleares, en los textos sobre VIH los blancos son generalmente referenciados como los mononucleares en su conjunto.
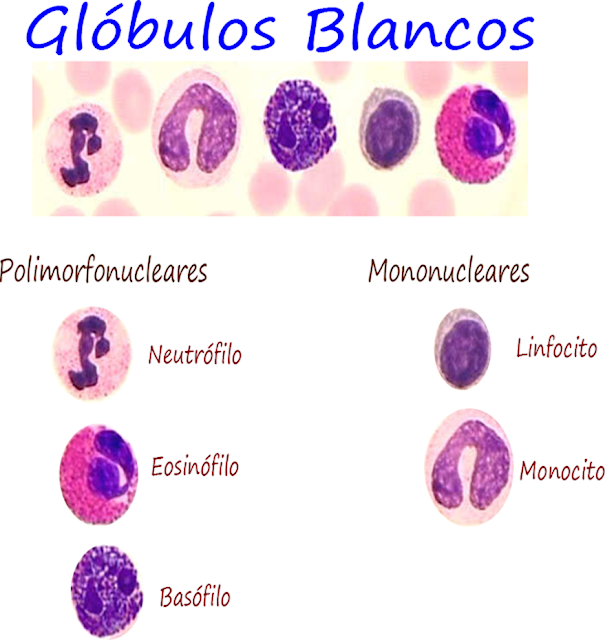
Figura 39. Los glóbulos blancos. En general los
leucocitos principales son 5, neutrófilos, eosinófilos, basófilos, linfocitos y
monocitos.
El VIH
posee como blanco a las células mononucleares, pero no todas, por lo cual
resulta conveniente describir sus tipos. En primera instancia los linfocitos Figura 40, Luego los descendientes de los
monocitos Figura 41.
El
trofismo/tropismo celular fue la tercera propiedad para clasificar los primeros
aislamientos del VIH- Todas las cepas del VIH-1 son capaces de reproducirse en
las células activadas “células mononucleádas de la sangre periférica como los
linfocitos, los monocitos y los macrófagos”.
Algunas pueden replicarse en cultivos sintéticos como MDM “Modified Dulbecco's Medium” y han sido clasificadas como cepas con tropismo de macrófago o cepas M-tróficas. Otros aislamientos iniciales del VIH-1 son capaces de infectar preferentemente las células T y ha sido designada como T-tróficas. Otros aislamientos primarios poseen la capacidad de infectar sin preferencia alguna cualquiera de los linajes del sistema inmune, ya sea el linaje de los linfocitos T o el linaje de los monocitos. Adicionalmente se encontró una asociación ya que las cepas lentas y de baja producción tienden a ser también las M-tróficas, mientras que las cepas rápidas y de alta producción tienden a ser T-tróficas.
Figura 40. Los linfocitos se ven iguales. Se resalta la población de linfocitos atacados por el VIH, en este caso únicamente los linfocitos con el receptor CD4 resultan atacados.
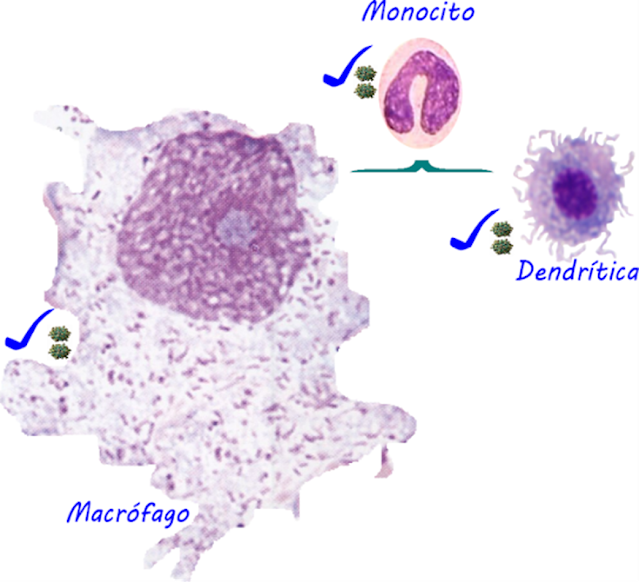
Figura 41. Los monocitos si se ven diferentes. A diferencia
de la línea linfocitaria, la monocitaria si experimenta grandes cambios en su
activación, el problema es que todas, incluso el precursor monocito posee el
receptor CD en sus membranas, lo cual los hace vulnerables al ataque del VIH.
Aparentemente
las clasificaciones del trofismo no tenían en cuenta a las cepas que atacan a
las microgliaes, sin embargo, debido a que estas son afectadas en las etapas
terminales, las cepas que las atacan son T-tróficas, ya que estas son las más
comunes en la etapa de SIDA.
Con el
descubrimiento de que receptores de quimioquinas alfa y beta sirven como un
segundo requisito de acceso a la célula blanco para que el VIH pueda infectar,
los protocolos de clasificación fueron alterados a un sistema mucho más
sistemático, la infección del VIH será ahora clasificada en base al código del
correceptor y no a cualidades variables como la velocidad de la infección.
A parte
del receptor CD4 el VIH requiere uno o cualquiera de dos receptores de
citoquinas. Estos receptores son proteínas G acopladas a un activador –el
receptor de citoquinas –normalmente las citoquinas son los señalizadores de
emergencia en el sistema inmune. Esto implica que la otra parte de importancia
de la proteína gp160 que es altamente conservada en los VIH es un homólogo de
citoquinas.
Los dos
receptores acoplados a una proteína G son denominados CCR5 y CXCR4. Las cepas
que emplean el receptor CCR5 son denominadas VIH-1 R5, mientras que las cepas
que emplean el coreceptor CXCR4 son denominadas VIH-1 X4. A parte de los dos
grupos emergió uno nuevo –uno transicional –intermedio que se caracteriza por
un tropismo dual y que explica los casos de una velocidad y productividad
intermedios llamado R5/X4.
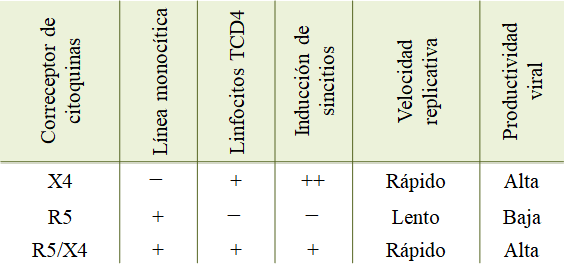
En la
siguiente tabla de plantea un resumen del tropismo del VIH-1. Cabe resaltar que
existen excepciones. Por ejemplo, algunos precursores linfocitarios puedes
expresar los dos receptores de citoquinas y por lo tanto, ser atacados por
versiones del VIH-1 R5. Un aspecto curioso sobre la investigación del VIH. Por
lo general los primeros intentos de aislar el VIH emplearon células T
cancerígenas para investigación debido a que pueden ser cultivadas a grandes
velocidades.
Sin
embargo, como cualquier linfocito T, estos no expresan el receptor CCR5, por lo
cual un cultivo de etapa aguda del VIH será incapaz de infectar al cultivo
arrojando un falso negativo. Esto se debe a que las infecciones iniciales son
causadas por la versión R5 del virus el cual necesita el receptor CCR5 presente
en la línea monocítica.
El correceptor de quimioquinas del tipo 5 conocido en inglés por los códigos CCR5 o CD195. Es una proteína de la superficie de las células blancas del sistema inmune que se encuentra involucrada como receptor de quimioquinas "también llamadas citocinas". Las quimioquinas son moléculas promiscuas –no específicas y por lo tanto poco diversas –que dirigen la activación de las células del sistema inmune, así como la activación y proliferación del mismo, en últimas son una señal de alarma para el sistema inmune. Específicamente, permite los linfocitos T y a los monocitos y sus descendientes ser atraídos a los tejidos donde se encuentran causados por virus, cáncer, bacterias, hongos o parásitos eucarióticos.
Figura 42. Los correceptores más
importantes para la infección por VIH.
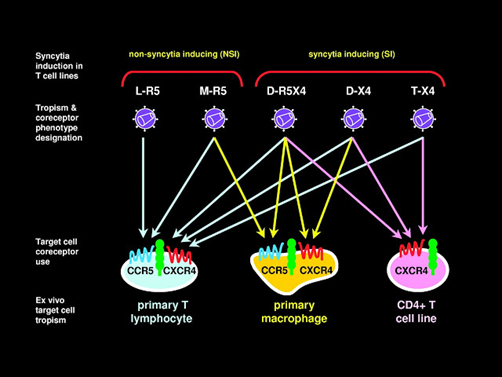
Tabla 3. Clasificación de la infección por VIH-1, por tropismo y fenotipo infeccioso.
El
correceptor CCR5 pertenece al grupo de receptores que quimioquinas beta, una
familia de proteínas integrales de la membrana, el cual se encuentra acoplado a
un dominio externo de un efector tipo G. Las proteínas G transfieren señales
desde el exterior de la célula al interior, son muy versátiles ya que lo único
que alteran es el receptor, dicho receptor puede ser modificado para activarse
por luz –para la visión –o ser activado por hormonas –como es el caso de la
reproducción.
CCR5 es
expresada de forma predominante en los linfocitos T inmaduros, pero es mucho
más importante los macrófagos y células dendríticas. Las células microgliales
expresa ambas, así como otro correceptor menos famoso para la infección del VIH
llamado CCR3, pero aparentemente las células microgliales son atacadas gracias
a su receptor CCR5, lo cual crea una paradoja, esto es debido a que en ese
contexto las microgliales deberían ser atacadas en la etapa aguda de la
infección.
Las
cepas del VIH afines al receptor CCR5 son denominadas cepas R5 y atacan
preferentemente a las células del linaje del monocito, es decir monocitos,
macrófagos y dendríticas, generalmente son clasificadas como cepas M-tropicas.
Estas cepas se reproducen lentamente, producen muy poca carga viral por célula
afectada y no forman sincitios. Los sincitios son células que expresan
receptores del VIH que inducen a interactuar con otras del mismo tipo
fusionándose, el producto son células gigantes polinucleadas con una alta
producción vírica.
Algunos individuos poseen una deleción de 32 pares de bases llamada delta 32 en el gen que codifica el receptor CCR5. Si el individuo es homocigoto delta 32, su línea monocitaria se hace fuertemente resistente al ingreso del VIH. Esto es posiblemente un arma de doble filo, un caso ha reportado que un individuo delta 32 homocigoto fue infectado por una cepa dual R5/X4, sufriendo de una rápida eliminación de sus linfocitos T CD4, esta es sin embargo una excepción, pero demuestra el efecto de la carrera armamentista de la Selección Natural.
Figura 43. La peste negra.
Aparentemente Yersinia pestis tiene un
mecanismo de ingreso a la célula dependiente al receptor CCR5, lo cual provocó
la generación de mutantes para este receptor, especialmente en Europa, donde
esta bacteria generó una grave epidemia llamada la peste negra.
La
prevalencia de la mutación Delta-32 se encuentra en países del norte de Europa,
la cual ayuda a que varios pacientes desarrollen lentamente la etapa de SIDA.
Por lo general, debido a las rutas de infección, las primeras cepas que
infectan a las personas son del tipo R5, con lo cual ser un mutante homocigoto
Delta-32 es una enorme ventaja evolutiva. Los individuos heterocigotos delta 32
tienden a ser progresivos lentos, es decir, son afectados por el VIH pero su
etapa de latencia es muy prolongada. En este sentido la mutación tiende a
convertir al VIH en un comensal.
Otras
mutaciones han sido reportadas para el gen CCR5 o para las citoquinas con las
cuales el VIH-1 compite para acoplarse. Algunas veces se trata de
polimorfismos, es decir de variantes informacionales como es el caso del
polimorfismo 59353-C del CCR5.
Algunos
individuos de progresión lenta, muy lenta o que han convertido el VIH en un
comensal poseen versiones modificadas de varias quimioquinas que activan al
receptor CCR5 compitiendo de forma eficiente con el VIH e impidiendo que su
carga viral sea muy alta de forma permanente.
Existe
una tasa representativa de individuos en la población con estas mutaciones, las
cuales reducen la probabilidad de infección del VIH, el problema nuevamente son
las cepas duales y la posibilidad de una cepa X4.
Mucho
de lo dicho ya en el receptor CCR5 aplica para este en términos de estructura
–se trata de un receptor acoplado a una proteína G –sin embargo, el receptor
CXCR4 posee una característica diferente, es un factor de fusión. A las cepas
que emplean este correceptor se las llama X4. En este sentido favorece la
función de la célula blanco con el VIH o con una célula infectada en producción
de receptores GP160. Y esto es justamente lo que las hace tan peligrosas, la
versión X4 puede infectar a otras células T CD4 no solo en estado de virión,
también cuando está al interior de una célula.
Las
células productos de la función se las llama sincitios y se caracterizan por
una alta producción de viriones, productor de la labor combinada de varios
núcleos de forma simultánea. Las cepas X4 emergen naturalmente de una población
R5 durante los años de la latencia, y el incremento de su prevalencia está asociado
al desarrollo de la etapa de SIDA. Al igual que con las cepas R5 algunos
individuos de la población poseen mutaciones que inhabilitan la expresión
adecuada del receptor CXCR4 haciendo que la progresión a etapa de SIDA sea
lenta o no se dé. Las razones para que las X4 emerjan a partir de las R5 se
desconocen en gran medida en la actualidad, lo que sí se sabe es que si una
persona es infectada con una cepa X4 la progresión de la infección será más
rápida.
La
llave de entrada del VIH se denomina gp160, una proteína compuesta por dos
subunidades, gp41 y gp120. Gp41 actúa como un tallo o grúa móvil, que cambiará
de forma cuando gp120 realice su segundo cambio conformacional. Por su parte,
gp120 puede ser considerada como los dientes de la llave, esta está conformada
para acoplarse a las dos guardas de la célula que va a atacar.
La
primera guarda es el receptor CD4, cuando GP120 se acopla a este receptor
cambia su estructura nativa –cambio denominado enmascaramiento conformacional
–lo cual permite la aparición de un segundo dominio que interactúa con un
correceptor, los principales con CXCR4 y CCR5 pero existen otros de menor
importancia. Los correceptores son la segunda guarda y una vez GP120 se ha
acoplado a estas dos guardas induce que GP41 haga ingresar al virión mediante
la fusión de las membranas.
Los
linfocitos B actúan contra el VIH produciendo anticuerpos anti gp120 en estado
nativo. Sin embargo existen dos
problemas con respecto a esta respuesta inmune inicial. La primera es el tiempo
que tarda la activación del linfocito B específico, y el tiempo de retraso con
respecto a la hipermutación somática. La activación del sistema inmune y la
mejora de la especificidad vía hipermutación somática tiene un tiempo de
retraso de unas dos semanas o más, tiempo en el cual el VIH se arraiga en el
sistema inmune del anfitrión.
El
segundo problema es que estos anticuerpos han evolucionado para atacar la
estructura nativa, pero una vez GP120 ha hecho contacto con CD4 esta estructura
nativa cambia y los anticuerpos ya no la reconocen. Este proceso es denominado
enmascaramiento conformacional.
Una vez
que GP120 se ha acoplado al receptor y el correceptor, GP41 cambia de forma,
jalando el virión hacia la célula blanco. Este proceso se facilita si el
receptor es la fusina CXCR4, la cual también jala la membrana del virus hacia
la célula acelerando la fusión. Una vez que la célula anfitriona empieza a
expresar las proteínas de la membrana del virus, su propia membrana se llena de
la proteína GP160 lo cual implica que puede interactuar con otras células. Para el caso de la cepa X4 la consecuencia es
que la célula anfitriona infectada puede jalar a otras células blanco
fusionándose con ellas creando una nueva célula más grande y con un potencial
para crear viriones más importante, estas células polinucleadas son llamadas
sincitios.
Cerca del 90% de las nuevas infecciones son por la cepa R5 debido a contacto sexual, mientras que la X4 requiere de contacto directo de sangre que contenga los linfocitos T CD4 que la poseen. Una vez que el virión ha ingresado a la célula los anticuerpos son inefectivos, pero los linfocitos T CD8+ se convierten en su principal amenaza junto con las células asesinas naturales NK.




No hay comentarios:
Publicar un comentario